导致中国人喝酒脸红的基因突变,还会增加心脏病风险,华人团队找到潜在治疗药物

(图片来源:摄图网)
作者|王聪 来源|生物世界(ID:ibioworld)
携带ALDH2基因突变的人在喝酒或饮用含酒精饮料时,会出现面部发红的症状。这是因为,ALDH2基因突变导致乙醛脱氢酶2的活性大大降低,从而导致酒精的中间代谢产物乙醛的积累,进而导致面部发红等症状。
全世界有大约8%的人携带这种基因突变,其中主要是东亚人群,因此,喝酒脸红的现象有时也被称为“亚洲红”。除了导致喝酒脸红,之前的研究显示,携带这种基因突变的人患冠状动脉疾病的风险显著上升。
2023年1月25日,斯坦福大学吴庆明(Joseph C. Wu)团队在 Science 子刊 Science Translational Medicine 上发表了题为:SGLT2 inhibitor ameliorates endothelial dysfunction associated with the common ALDH2 alcohol flushing variant 的研究论文。
该研究表明,导致喝酒后面部发红的ALDH2基因突变通过诱导内皮细胞功能障碍,从而增加冠状动脉疾病(CAD)风险。更重要的是,该研究还发现了一种已获得FDA批准上市的药物SGLT2抑制剂Empagliflozin(恩格列净,2型糖尿病药物)能够预防和治疗ALDH2基因突变相关内皮细胞功能障碍


吴庆明(Joseph C. Wu)
吴博士是斯坦福大学教授,自2013年以来担任斯坦福心血管研究所所长,是全球心脏病学领域论文被引用次数最多的学者之一,在 Nature、Cell、Science,及 Nature Medicine、Science Translational Medicine、Cell Stem Cell、PNAS、Circulation、JACC、EHJ 等等级学术期刊发表多篇学术论文。
根据世界卫生组织(WHO)的数据,冠状动脉疾病(CAD)是全球死亡的主要原因,每年造成约900万人死亡。由于人口老龄化,以及缺乏有效预防和治疗CAD的创新策略,CAD的全球患病率正在上升。通过了解遗传变异的生理机制和因果关系,对具有遗传变异的CAD患者进行精准医疗有望成为一种更有效的预防和治疗新方法。
冠状动脉疾病(CAD)是一种由多种遗传和环境因素相互作用引起的复杂疾病,通过全基因组关联研究(GWAS),已发现数百个与CAD相关的基因组位点。
喝酒或饮用含酒精饮料后,酒精(乙醇)在人体内的代谢过程是乙醇→乙醛→乙酸→二氧化碳和水,其中ALDH2基因编码的乙醛脱氢酶2,是酒精代谢的关键酶,负责将对人体有毒的乙醛代谢为相对安全的乙酸。

而在东亚人中,ALDH2基因突变普遍存在,这导致其活性显著降低,从而导致喝酒后的乙醛积累,出现面部发红的症状。其中,ALDH2基因的rs671位点变异非常常见(也被表示为ALDH2*2),这一突变导致该酶的第504位的谷氨酸被赖氨酸替换(E504K),这一突变在我国非常普遍,约占总人数的30%-50%,尤其是在我国东南部地区。
之前的研究显示,ALDH2*2基因突变携带者不仅ALDH2酶活性显著降低,还与各种神经、心血管和皮肤疾病有关,还会导致药物代谢异常,以及胃癌等癌症发病风险上升。
2017年12月,江苏省人民医院李妍妍等人在 Journal of Cellular and Molecular Medicine 期刊发表了一篇Meta分析论文【2】,该论文显示,ALDH2*2基因突变与冠状动脉疾病(CAD)风险增加48%相关。
然而,ALDH2*2与冠状动脉疾病(CAD)发病之间的潜在机制尚不清楚,这为预防和治疗ALDH2*2相关冠状动脉疾病(CAD)造成了障碍。因此,确定ALDH2*2和饮酒对CAD的联合影响,从而制定预防策略,这对降低ALDH2*2携带者的冠状动脉疾病(CAD)风险很重要。
在这项最新研究中,研究团队分析了日本生物数据库的患者数据,寻找ALDH2基因突变与冠状动脉疾病(CAD)风险增加之间的联系,并测试了几种药物,以确定它们是否能够降低冠状动脉疾病(CAD)风险。
研究团队分析了29319名冠状动脉疾病(CAD)患者的数据,并将其与183134名对照组进行比较。研究团队发现,ALDH2基因突变和冠状动脉疾病(CAD)之间的强烈联系。他们还发现,即使少量饮酒(1标准杯)也会对血管内皮细胞功能产生显著影响。而那些重度饮酒者患冠状动脉疾病(CAD)的风险是普通人群的4倍。
研究团队还发现了ALDH2*2携带者的血管内皮存在问题,内皮细胞(ECs)是血管壁的重要组成部分,通过调节血管张力和结构在维持心血管稳态中发挥重要作用。内皮细胞功能障碍在冠状动脉疾病(CAD)发病的各个阶段发挥着决定性作用。ALDH2*2与内皮细胞功能障碍相关,但具体机制尚不清楚。
研究团队利用人诱导多能干细胞分化来源的血管内皮细胞(iPSC-EC),并使用CRISPR-Cas9基因编辑技术构建了ALDH2*2 iPSC-EC,从而在体外模拟ALDH2*2诱导的内皮细胞功能障碍。结果显示,ALDH2*2会导致内皮细胞氧化应激和炎症标志物增加,一氧化氮(NO)产生和血管形成能力下降,而酒精(乙醇)暴露进一步加剧了这些情况。
接下来,研究团队评估了8种药物的治疗效果,这些药物已知能够减少炎症、降低活性氧(ROS)和增加一氧化氮(NO),其中7种已获FDA批准,还有1种是ALDH2激活剂Alda-1。
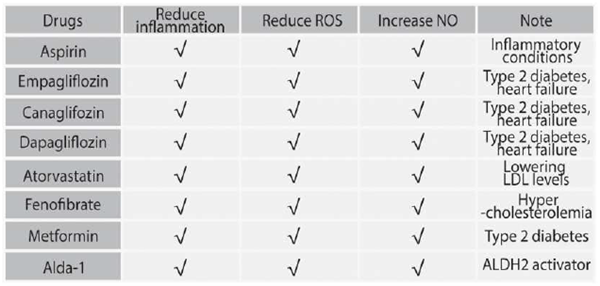
结果显示,SLGT2抑制剂(SGLT2i),例如Empagliflozin(恩格列净,一种2型糖尿病药物)可以缓解ALDH2*2相关内皮细胞功能障碍。SGLT-2,即钠-葡萄糖协同转运蛋白2,负责肾脏对葡萄糖的重吸收。
研究团队在ALDH2*2基因敲入小鼠模型上进行了进一步验证,结果显示,Empagliflozin可在体内缓解ALDH2*2介导的血管功能障碍。从机制上来说,Empagliflozin抑制了Na+/H+交换器1(NHE-1),激活AKT激酶和内皮细胞一氧化氮(NO)合成酶(eNOS)通路,从而改善ALDH2*2诱导的血管内皮细胞功能障碍。
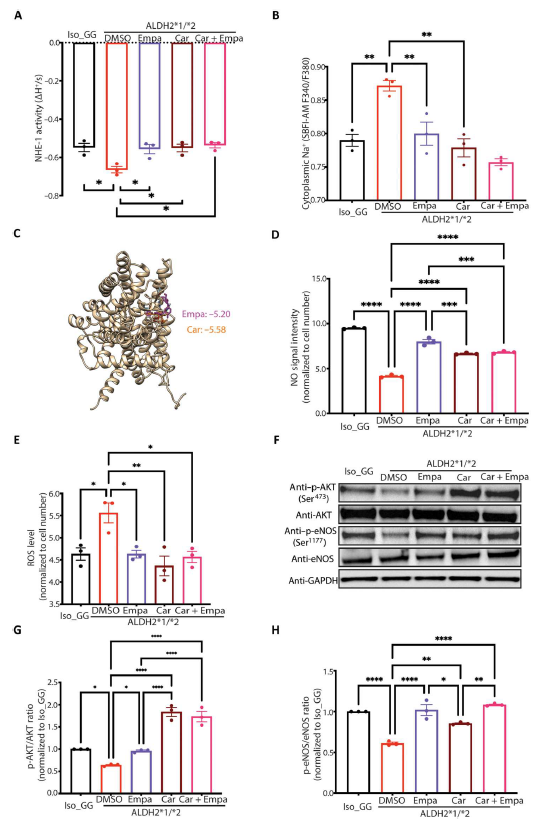
总的来说,这些结果表明,ALDH2*2基因突变诱导了内皮细胞功能障碍,从而增加了冠状动脉疾病(CAD)风险,而SLGT2抑制剂(SGLT2i)可以预防和缓解这种内皮细胞功能障碍。如果这类药物在人类身上起到类似的作用,那么它们很可能被用于降低ALDH2基因突变携带者患冠状动脉疾病(CAD)的风险。
论文链接:
https://www.science.org/doi/10.1126/scitranslmed.abp9952
https://onlinelibrary.wiley.com/doi/10.1111/jcmm.13443
编者按:本文转载自微信公众号:生物世界(ID:ibioworld),作者:王聪
品牌、内容合作请点这里:寻求合作 ››

前瞻经济学人
专注于中国各行业市场分析、未来发展趋势等。扫一扫立即关注。




























