干细胞疗法,“永生”之舟?

(图片来源:摄图网)
作者|青栎 来源|医曜
生老病死是任何人都无法逃脱的自然法则。无数帝王为了实现永生的夙愿,不惜炼丹试药,但最终都只不过是过眼云烟。
尽管目前的科技水平无法使人类达到长生不老的地步,但科学的进步促使人类寿命不断增加也是不争的事实。如果科技带来的延寿速度快于自然衰老的速度,那么就相当于达到了“生命逃逸速度”,也就是说人类将在不断延寿的过程中达到永生。
一场关于“永生”的全球竞赛,其实早已拉开序幕。
01
重建生命的神奇“魔法”
干细胞是一类具有自我复制和多向分化潜能的细胞群体,被医学界称为“万用细胞”,主要来源于脐带血、骨髓、外周血、胚胎及牙髓等,在特定的条件或者特定的信号诱导下能够分化成多种功能细胞或组织器官。
追根溯源,最早提出“干细胞”一词的是德国生物学家Ernst Haeckel,他于1868年首次用其来描述受精卵产生生物体所有细胞的特性。基于此,医学界逐渐开始尝试利用干细胞进行治疗,也就是利用干细胞或干细胞衍生的细胞,以特殊技术移植到体内替代或分泌活性因子修复病人受损的细胞、组织或器官。
尽管人类很早就进行了尝试,但直至90年后才真正地取得了实质性的进展。1958年,法国肿瘤学家George Mathe首次进行了一次异体干细胞移植,使用骨髓移植治疗了6名意外暴露于放射性物质的研究人员,其中有5例获得成功。
正是这一里程碑式的案例,让业界看到了干细胞疗法的真正价值。十年后的1968年,Gatti等人成功地为一位重症联合免疫缺陷患儿实施了HLA相合的同胞间骨髓移植,自此之后干细胞疗法便开始驶入发展快车道。
然而,干细胞疗法一直因伦理问题而受到大众的质疑。一些人认为人类胚胎从受精那一刻起就拥有与成人相同的权利,因此使用人类胚胎进行研究是不道德的。
直到2007年,日本科学家山中伸弥使用人皮肤细胞经重编程获得了具有分化潜能的诱导多能干细胞(iPSCs),该研究一定程度缓和了胚胎干细胞研究涉及的宗教、伦理问题,并于2012年获得了诺贝尔医学或生理学奖。
由于干细胞种类繁多,与之对应的治疗机理也各不相同,大体可以分为以下三类:
◆体内分化,体内治疗
在体外进行简单分离后,将干细胞直接移植入体内修复损伤部位。临床上主要用于放/化疗之后补充造血干细胞,进而重塑整个造血系统和免疫系统。
◆体外分化,替代治疗
通过体外大量扩增并诱导分化,将干细胞变成特定的功能细胞,再移植入体内,对损伤部位修复。最具代表性的是多能干细胞治疗,如利用诱导多能干细胞治疗视网膜黄斑变性、帕森病、心脏衰竭、脊髓损伤等疾病。此外,这一原理还应用在很多干细胞衍生技术,如3D细胞打印技术、3D培养技术,微组织技术、类器官技术等。
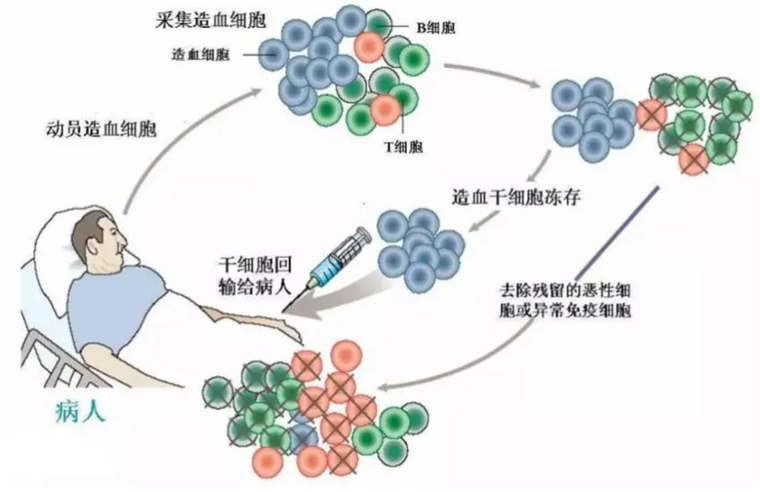
图:干细胞疗法简单示意图
◆分泌效应,信号引导
大部分干细胞进入体内并不会分化成损伤部位的细胞,而是通过分泌活性因(包括细胞因子、外囊泡等信号分子),调节免疫或促进组织修复。例如,间充质干细胞通过静脉输注后,一开始绝大部分都会滞留在肺部,之后部分细胞迁移至其他组织器官以及损伤部位,在过程中释放各种活性因子(包括细胞因子,外囊泡等)。
以结果而论,干细胞疗法无疑是成功的,为一些传统医学难以治愈的疑难病症带来了新的曙光。
如神经系统疾病的帕金森病和阿尔茨海默病,就有希望通过干细胞分化为神经细胞,替代受损的神经元,有望改善患者的认知和运动功能;再比如心血管疾病领域,干细胞能够分化为心肌细胞,修复受损的心肌组织;在糖尿病治疗中,干细胞可分化为胰岛细胞,分泌胰岛素,为1型糖尿病患者提供一种潜在的根治方法,同时也有助于改善2型糖尿病患者的胰岛功能。
干细胞,相当于对人体细胞的一次重构,如果将人体的细胞全部替换,那是否就相当于一次新生呢?
02
全球研发热潮
基于干细胞疗法强大的应用潜力,这一赛道的关注度也在持续升高。
目前,根据发育阶段来源可将干细胞分为胚胎干细胞、成体干细胞以及iPS干细胞三类。同时,根据分化潜能的大小,干细胞又可分为全能干细胞、多能干细胞和单能干细胞三类。
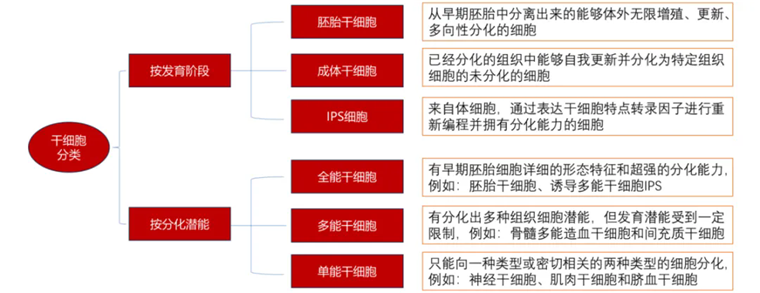
图:干细胞疗法分类,来源:民生证券
全能干细胞(如胚胎干细胞)可分化成为机体的任何细胞,分化潜力最大,无疑是人体最佳的修复材料。然而,却受限于潜在的胚胎瘤风险和社会伦理问题。
因此,多能干细胞疗法是当下干细胞研发的重点。虽然多能干细胞并没有全能干细胞那样强大的分化能力,但也具有多向分化潜能,尤其是间充质干细胞更是现阶段科学研究与临床应用最多的干细胞。
据不完全统计,目前全球已上市的干细胞疗法药物共25款,其中有8款属于间充质干细胞疗法,11款属于造血干细胞疗法,其中美国上市的药品数量最多,共10款。在我国,造血干细胞被视为器官移植监管,而不是作为药物监管,因此我们寻找这一原则,并不将造血干细胞疗法计算在内。
在研产品方面,根据智慧芽数据,截至2023年2月底,全球正在开发的干细胞疗法药物1041款,全球开展的临床试验1811项,其中临床前246项,临床I期95项,临床II期76项,临床III期26项。药物类型上,间充质干细胞疗法占比高达60%,造血干细胞疗法占比11.5%,诱导多能干细胞疗法占比1.9%,神经干细胞疗法占比1.9%,其余干细胞疗法占比24.7%。
从覆盖的适应症方面,目前的临床研究涉及适应症包括自身免疫性疾病(类风湿关节炎、强直性脊柱炎、银屑病、移植物抗宿主病)、代谢性疾病(糖尿病足溃疡)、骨关节病(骨关节炎)、呼吸系统疾病(肺纤维化、肺损伤)、消化系统疾病(肝衰竭、克罗恩病)、心脑血管疾病(脑卒中)等病种,并仍在不断扩展边界。
从地区分布来看,美国拥有世界顶尖水平的高校、研究机构及医疗机构,是全球干细胞医疗第一大技术来源国,专利申请量占全球干细胞医疗专利总申请量的28%,一直占据着主导地位。同时,由于美国的私人医疗市场发达,为干细胞疗法的商业化应用提供了广阔的空间,全球获批的脐血造血干细胞产品中,80%来自美国。
不过,由于严格的FDA审核要求,至今还没有批准任何间充质干细胞疗法上市。相反欧洲、日本、韩国等国家和地区对于新兴医疗技术和治疗方法秉持着开放的态度,越来越多的干细胞产品成功上市。
今年7月,Mesoblast公司向FDA重新提交了Ryoncil的上市申请,用于治疗类固醇难治性急性移植物抗宿主病(SR-aGVHD)的儿童,该申请的PDUFA日期为2025年1月7日。Ryoncil是一种间充质干细胞,通过抑制T细胞增殖,和下调促炎细胞因子和干扰素的产生,来调节T细胞介导的炎症反应。如果Ryoncil顺利获批,那么将成为美国第一类获批的干细胞创新疗法。
美国市场之外,韩国已经批准5款间充质干细胞疗法,包括Queencell、Cupistem等;日本作为iPSC的开创者也紧随其后,批准了3款间充质干细胞疗法,包括Temcell、Stemirac等;欧洲也批准了Holoclar和Alofisel两款干细胞药物。
以全球干细胞产业发展速度看,其并没有遵循创新药FDA“唯我独尊”的趋势,从原本美国一家独大的局面开始朝着其他国家和地区均衡化的方向发展。这也从侧面表明,全球各国对于干细胞疗法的重视程度。
03
下一个必争之地?
如果说未来有什么产业会如同“芯片”一样成为大国博弈的焦点,干细胞疗法在内的生物技术绝对占有一席之地。
干细胞曾经连续两次被《科学》(Science)杂志列为世界十大科学问题之首,干细胞研究还曾在2007年和2011年获得诺贝尔生理学和医学奖。
通过研究干细胞不仅能够攻克各种疾病、延缓衰老、增强免疫的潜力,而且还有助于深入了解生命的起源、发育以及疾病的发生发展过程,从而推动基础医学的发展,促进医学技术的创新。
同时,干细胞产业涉及生物医药、医疗器械、健康管理等多个领域,是一个具有高附加值的产业。发展干细胞产业可以带动相关产业的发展,提升国家的产业竞争力,促进经济的可持续发展。因此,干细胞疗法作为体现国家意志、服务国家需求、代表国家科技创新最高水平的战略科技力量,越来越受到全球各个大国的重视。
美国为了维持其在干细胞疗法领域的优势地位,曾在2022年9月,签署《关于促进生物技术和生物制造创新以建立可持续、安全和有保障的美国生物经济的行政命令》,旨在保护核心技术,号召生物制造回流美国本土,以减少对外部的依赖。
特朗普的胜选,更是为干细胞疗法在美国的发展打下一剂强心针。2018年,特朗普签署了《尝试权法案》,该法案旨在帮助绝症患者获得未经美国 FDA 完全批准的药物治疗,其中也包括一些处于试验阶段的干细胞疗法。在其首个总统任期内,特朗普就通过国会演讲等多种途径表达了对干细胞治疗的支持与认可。他还强调,FDA漫长且繁琐的审批流程会阻碍许多研究成果应用到真正有需要的领域。
如今特朗普再次上台,或将进一步提升干细胞疗法的战略地位,为其设置更为宽松的政策环境,同时可能继续强化自身在医院产业的霸主地位。
我国对干细胞疗法也高度重视。早在2016年,就已经把重点发展 “干细胞与再生医学” 纳入《“健康中国 2030”规划纲要》之中。不仅如此,在《十四五规划》里也清晰地将免疫细胞治疗、干细胞治疗、基因治疗产品等列入了规划内容。
从科研资金支持上看,2016年—2022年,中央财政连续多年拨款总计近40亿元,支持了众多干细胞研究项目,涉及干细胞的基础研究、临床应用研究等多个方面,推动了干细胞疗法的科研进展。
在监管制度层面,为了激励干细胞产业发展,我国干细胞政策实行了“双轨制”,直接对标美国相关制度。在这种模式下,干细胞既能够以医疗技术的形式申报备案,也可以当作药品来申请上市,这大大加快了干细胞临床转化的速度。
政策和市场的双向推动下,近年来,我国干细胞研究已跃居世界前列,在该领域论文发表数量及专利申请量已连续5年位居世界第二,干细胞备案项目和干细胞IND注册受理项目数量成倍增长,通过新药注册申报途径研发的干细胞临床管线持续增加。
截至2023年底,我国已有106款干细胞药物的临床试验申请获得CDE受理,其中79款为默认许可。2024年8月底,北京药监局核发了全国首张干细胞药物的《药品生产许可证》,干细胞疗法迈出了从研发到生产的关键一步。
干细胞疗法正站在时代的风口浪尖,它承载着人类对健康和生命延续的无限憧憬。在全球竞争与合作的大舞台上,各国都在这片充满希望的领域里奋勇前行。无论是美国的战略保护与推进,还是中国的积极投入与发展,都预示着干细胞疗法将在未来全球生物医药版图中占据关键地位。
编者按:本文转载自微信公众号:医曜,作者:青栎
品牌、内容合作请点这里:寻求合作 ››

前瞻经济学人
专注于中国各行业市场分析、未来发展趋势等。扫一扫立即关注。




























